Turicibacter sanguinis: Ein sehr seltener Infektionserreger
TR 02.03.2022
Ein 53 Jahre alter Patient wird mit Verdacht auf Sepsis auf die Intensivstation eingeliefert. Bei der initialen Laboruntersuchung fällt neben deutlich erhöhen Leberwerten inbesondere ein sehr hoher Procalcitoninwert auf (23,5 µg/l). Der initiale Verdacht auf eine Cholangitis veranlasst zu einer antibiotischen Therapie mit Ceftriaxon plus Metronidazol. Mehrere bei Aufnahme entnommene anaerobe Blutkulturen weisen bereits am Folgetag Wachstum von grampositiven Stäbchen mit subterminalen Sporen auf (Abb.). Ein Differenzierungsversuch mit MALDI-TOF bleibt wiederholt ohne Ergebnis. Die 16s-Sequenzierung zeigt eine weitgehende Übereinstimmung mit der Sequenz von Turicibacter sanguinis.
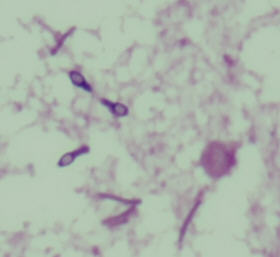
Abb. Subterminale Sporen von Turicibacter sanguinis in der Blutkultur. Foto: Alexander Holzer, Lab. Enders
Unter der Antibiotikatherapie gehen die Entzündungswerte rasch zurück. Der Verdacht auf Cholangitis bestätigt sich nicht. Als mutmaßlicher Fokus für die Bakteriämie stellt sich ein fistelnder präsakraler Abszess heraus, der chirurgisch behandelt wird. Wenige Tage später kann der Patient in die ambulante Weiterbehandlung entlassen werden.
Turicibacter sanguinis wurde erstmals 2002 als neue Spezies in einem neuen Genus beschrieben (doi: 10.1099/00207713-52-4-1263). Das beschriebene Isolat war aus dem Blut eines Patienten mit Appendizitis angezüchtet worden. Im Anschluss wurde der Erreger mehrfach aus Faeces von Mensch und Tier isoliert. Heute wird Turicibacter sanguinis als Vertreter der Darmmikrobiota angesehen, der nur in Einzelfällen als Verursacher von Infektionen auftritt. Unser Fall ist der dritte in der Literatur beschriebene Nachweis des Erregers in der Blutkultur.
Während Turicibacter sanguinis ursprünglich als nicht sporenbildender Erreger beschrieben wurde, konnte später gezeigt werden, daß die Spezies in der Lage ist, Endosporen zu bilden (doi:10.1038/nature17645). Ungewöhnlich ist jedoch, dass unser Isolat im Blutkulturmedium Sporen ausgebildet hat. In der Regel sporulieren Bakterien bevorzugt in Minimalnährmedien.
Canibacter oris: Neuer Verursacher von Infektionen nach Tierbissen
TR 28.05.2021
Fall 1: Ein 61 Jahre alter Patient wird beim Spielen von einem jungen Hund in den linken Zeigefinger gebissen. Die geringgradige Verletzung nimmt er zunächst nicht ernst. Einige Tage später ist der Finger schmerzhaft geschwollen und gerötet. In einer Klinikambulanz wird ein Weichteilabszess festgestellt und eröffnet. Der Patient wird mit einer Antibiotikaverordnung wieder nach Hause entlassen. Einige Tage später ergibt die bakteriologische Kultur des Wundabstrichs Wachstum von Canibacter oris und Capnocytophaga species. Bei der Wiedervorstellung nach drei Tagen in der Ambulanz wird eine deutliche Befundbesserung vermerkt.
Fall 2: Eine 80-jährige Patientin wird von ihrem Hausarzt mit einer Phlegmone des rechten Handrückens in die Klinik eingewiesen. Sie berichtet, dass sie einige Tage zuvor von einer ihrer Katzen beim Füttern in die Hand gebissen wurde. Wegen des ausgeprägten Befundes und einer CRP-Erhöhung auf 45 mg/l wird die Patientin nach der Wundversorgung stationär mit Antibiotikainfusionen behandelt. In der bakteriologischen Kultur des Abstrichs werden Canibacter oris und Pasteurella multocida nachgewiesen. Einige Tage später kann die Patientin mit deutlich gebessertem Lokalbefund und rückläufigem CRP nach Hause entlassen werden. Die Antibiotikatherapie wird oral weitergeführt.
Hintergrund: Infizierte Tierbißwunden können zu schweren Gewebedefekten und zu systemischen Komplikationen führen (Sepsis, Endokarditis). Deshalb ist eine chirurgische Versorgung und eine Behandlung mit einem Breitspektrumantibiotikum (i.d.R. Aminopenicillin + Betalaktamasehemmer) obligatorisch. Verursacher der Infektionen sind meistens bakterielle Erreger aus der Mundflora des Tieres. Häufig findet man als typische Erreger Pasteurella multocida – seltener Capnocytophaga species. Canibacter oris wurde vor wenigen Jahren erstmals nachgewiesen und als bisher einzige Spezies einer neuen Gattung von grampositiven Erregern klassifiziert. Bisher wurden erst 2 Fälle von Wundinfektionen durch diesen Erreger beschrieben (Australien 2014, Speyer/Deutschland 2021). Die oben beschriebenen Fälle stammen aus den Jahren 2020 und 2021 (Raum Esslingen).
Candida orthopsilosis als Verursacher einer Fungämie
TR 26.2.2021
Eine 54-jährige Patientin mit chronischer Leber- und Nierenfunktionseinschränkung wurde wegen einer schweren bakteriellen Pneumonie invasiv beatmet und über mehrere Wochen mit verschiedenen Breitspektrum-Antibiotika behandelt. Im Verlauf kam es zu einer Sepsis, welche nicht mehr auf Antibiotika ansprach, obwohl keine multiresistenten bakteriellen Erreger nachweisbar waren.
In mehreren Blutkulturen wurde Candida orthopsilosis nachgewiesen. Der selbe Erreger ließ sich auch aus der Einstichstelle einer bereits vor Aufnahme vorhandenen PEG in hoher Keimzahl nachweisen. Vermutlich handelte es sich um den Focus der Infektion.
Trotz bereits begonnener antimykogramm-gerechter antimykotischer Therapie verstarb die Patientin.
Candida orthopsilosis ist ein seltener Verursacher von Fungämien. Betroffen sind in erster Linie Neugeborene und immunsupprimierte Erwachsene. Weitere Risikofaktoren sind parenterale Ernährung und intravasale Katheter.
Die Erreger sind fast immer empfindlich auf Azole und Echinocandine. Auch unter adäquater antimykotischer Therapie ist die Letalität hoch.
Letale Clostridien-Sepsis in der Schwangerschaft
TR 25.2.21
Eine 30 Jahre alte Patientin in der 38. Schwangerschaftswoche erlitt aus völliger Gesundheit einen hypovolämischen Schock. Wegen des Nachweises von reichlich freier Flüssigkeit im Abdomen wurde mit Verdacht auf eine Gefäßruptur umgehend laparotomiert. Man fand eine massive frische intra- und retroperitoneale Blutung, ausgehende von einer Ruptur der Milzkapsel und der linken Nierenarterie. Mutter und Kind verstarben.
Die Sektion der Mutter ergab das Bild einer Sepsis mit Multiorganversagen. Die Gewebe von Herz, Leber und Milz wiesen Gasbildung auf. Histologisch wurde zahlreiche Stäbchenbakterien nachgewiesen. Die bakteriologische Kultur eines intraoperativen Abstrichs zeigte Wachstum von Clostridium perfringens in hoher Keimzahl.
Clostridium perfringens ist der häufigste Verursacher von Gasbrand. Septische Verläufe in der Schwangerschaft wurden nur in Einzelfällen beschrieben.
Charakteristisch für die schwere Clostridiensepsis ist eine ausgeprägte intravasale Hämolyse und eine disseminierte intravasale Gerinnung, welche zum Multiorganversagen führen. Dafür verantwortlich ist das von Clostridium perfringens gebildete alpha- und theta-Toxin.
Risikofaktoren bei Schwangeren sind insbesondere invasive Maßnahmen wie Amniozentese und ein über längere Zeit bestehender Blasensprung. Weitere Risikofaktoren, unabhängig von einer Schwangerschaft, sind infizierte Wunden und invasive Maßnahmen im Bereich des Abdomens wie ERCP.
Im vorliegenden Fall konnten keine Risikofaktoren eruiert werden. Somit ist von einer spontanen Clostridiensepsis auszugehen. Als Infektionsherd der spontanen Clostridiensepsis kommen insbesondere Leberabszesse in Frage. Auch dafür gab es allerdings im beschriebenen Fall keinen Anhalt. Somit blieb die Infektionsgenese unklar.
[Die mikrobiologische Diagnose wurde in diesem Fall nicht im Labor Enders durchgeführt; die Angaben zu Klinik und Pathologie wurden im Rahmen einer Konsultation mitgeteilt]Erstmals Pseudomonas helleri in klinischem Material nachgewiesen
TR 22.7.20
Bei der routinemäßigen Kontrolluntersuchung wurde im Sputum einer 16-jährigen CF-Patienten neben anderen Erregern Pseudomonas helleri kulturell nachgewiesen. Die Identifizierung gelang mittels 16s-Sequenzierung. Ein Identifizierungsversuch mit MALDI-TOF hatte kein verwertbares Ergebnis erbracht. Der nächstliegende Treffer entsprach am ehesten dem Spektrum von Pseudomonas fragi.
P. helleri wurde 2016 erstmals von einer deutschen Arbeitsgruppe aus der Veterinärmedizin beschrieben. Diese konnte den Erreger in roher Kuhmilch nachweisen (DOI: 10.1099/ijsem.0.000852). Beim Menschen konnte die neue Spezies unseres Wissens bisher nicht nachgewiesen werden. Über die Pathogenität für Tier oder Mensch ist nichts bekannt, da bisher keine Erkrankungsfälle beschrieben worden sind. Somit ist die Relevanz des Erregers im vorliegenden Fall zunächst unklar.
Neisseria gonorrhoeae als Verursacher einer Tenosynoviitis
TR 22.7.20
Ein 51 Jahre alter Patient stellte sich mit Schmerzen in der linken Hand und Fieber vor. Die Hand war im Bereich des zweiten und dritten Strahls geschwollen und gerötet. Eine Verletzung war nicht erkennbar.
Da die Beschwerden zunahmen wurde die Hand operiert. Die bakteriologische Untersuchung eines intraoperativen Abstrichs ergab das Wachstum von Neisseria gonorrhoeae („Gonokokken“) in Reinkultur.
Der operative Eingriff und die antibiotische Behandlung mit Ceftriaxon führten zur Abheilung der Infektion.
Unklar blieb, auf welchem Weg die Gonokokken ins Gewebe der Hand gelangt waren. Prinzipiell wäre dies auf direktem Weg über eine Gewebeläsion im Bereich der Hand oder hämatogen ausgehend von einer Genitalinfektion möglich.
Ähnliche Fälle wurden in der medizinischen Literatur bisher nur vereinzelt beschrieben.
Lactobacillus delbrueckii: Ein seltener Verursacher von Harnwegsinfektionen
TR 23.7.20
Eine 47 Jahre alte ambulante Patientin mit bekannter Diabetes mellitus wurde wegen typischer Zystitisbeschwerden und dem Nachweis von Leukozytenesterase im Streifentest (Urin-Stix) mit Fosfomycin p.o. behandelt. Da eine Besserung ausblieb wurde 2 Tage später eine Untersuchung des Urinsediments veranlasst und eine bakteriologische Kultur auf einem Eintauchnährmedium in der Praxis angesetzt, sowie eine Therapie mit Cotrimoxazol verordnet.
Nach vorübergehender Beschwerdebesserung traten erneut Schmerzen auf. Da die Kultur auf dem Eintauchnährmedium kein Wachstum zeigte, obwohl im Urinsediment Leukozyten und Bakterien zu erkennen waren, wurde auf Anraten des Mikrobiologen eine Urinkultur im mikrobiologischen Labor veranlasst.
Die Kultur im mikrobiologischen Labor ergab das Wachstum von Lactobacillus delbrueckii in einer Keimzahl von > 100.000 KBE/ml in Reinkultur. Das Isolat wies eine Resistenz gegen Fosfomyin, Cotrimoxazol und Ciprofloxacin aus, war aber empfindlich auf Penicilline und Cephalosporine.
Die anschließende Behandlung mit Amoxicillin führte zu einem raschen Abklingen der Symptome. Kontrollurinsediment und Urinkultur waren im Anschluss ohne pathologischen Befund.
Laktobazillen sind Teil der Normalflora von Darm und Vagina und gelten als gering virulent. Als Verursacher von Harnwegsinfektionen kommen sie extrem selten vor. Neben unserem Fall wurde bisher nur eine weitere durch L. delbrueckii verursachte Harnwegsinfektion einer Frau beschrieben (https://jcm.asm.org/content/47/1/275). Da sich die Erreger auf den üblichen Tauchträgernährmedien nicht vermehren können, gelingt der Nachweis nur im mikrobiologischen Fachlabor.
L. delbrueckii ist in Probiotikazubereitungen und verschiedenen Molkereiprodukten enthalten. Leider liegen diesbezüglich keine Angaben von Seiten der Patientin vor.
